UDI - Mã định danh thiết bị duy nhất là gì?
Mã định danh thiết bị duy nhất (UDI) là một chuỗi ký tự duy nhất được sử dụng để phân biệt các thiết bị y tế. Cung cấp các thông tin chi tiết liên quan đến sản phẩm. Ví dụ như nhà sản xuất, loại thiết bị, ngày sản xuất,… UDI giúp xác định chính xác thiết bị và theo dõi truy xuất những thông tin quan trọng đến thiết bị, dễ dàng cho việc sử dụng và thu hồi sản phẩm.

1. Định nghĩa và cấu trúc của UDI
1.1 Định nghĩa
FDA đã thiết lập hệ thống nhận dạng thiết bị duy nhất (UDI) để xác định đầy đủ các thiết bị y tế thông qua việc phân phối và sử dụng ở Hoa Kỳ. Hệ thống nhận dạng thiết bị y tế duy nhất yêu cầu nhãn thiết bị y tế phải bao gồm mã nhận dạng thiết bị y tế duy nhất (UDI). Và yêu cầu nhà dán nhãn phải gửi thông tin sản phẩm liên quan đến thiết bị. tới Cơ sở dữ liệu nhận dạng thiết bị duy nhất toàn cầu (GUDID) của FDA trừ khi có ngoại lệ hoặc thay thế.
1.2 Cấu trúc
Mã định danh thiết bị duy nhất là mã số hoặc chữ và số duy nhất thường bao gồm các mã
- Mã nhận dạng thiết bị (DI). Là một phần cố định, bắt buộc của UDI để xác định nhãn và phiên bản hoặc kiểu máy cụ thể của thiết bị.
- Mã nhận dạng sản xuất (PI). Giúp xác định chính xác thiết bị bằng cách cung cấp thông tin khác nhau như lô, số sê-ri, ngày hết hạn, ngày sản xuất. Và mã nhận dạng riêng biệt được yêu cầu trong 21 CFR 1271.290© đối với tế bào, mô của người hoặc sản phẩm dựa trên tế bào và mô (HCT/P).
2. Làm cách nào để nhận biết UDI trên nhãn?
Để nhận biết được UDI trên nhãn thiết bị y tế bạn có thể dựa vô một số thông tin sau đây:
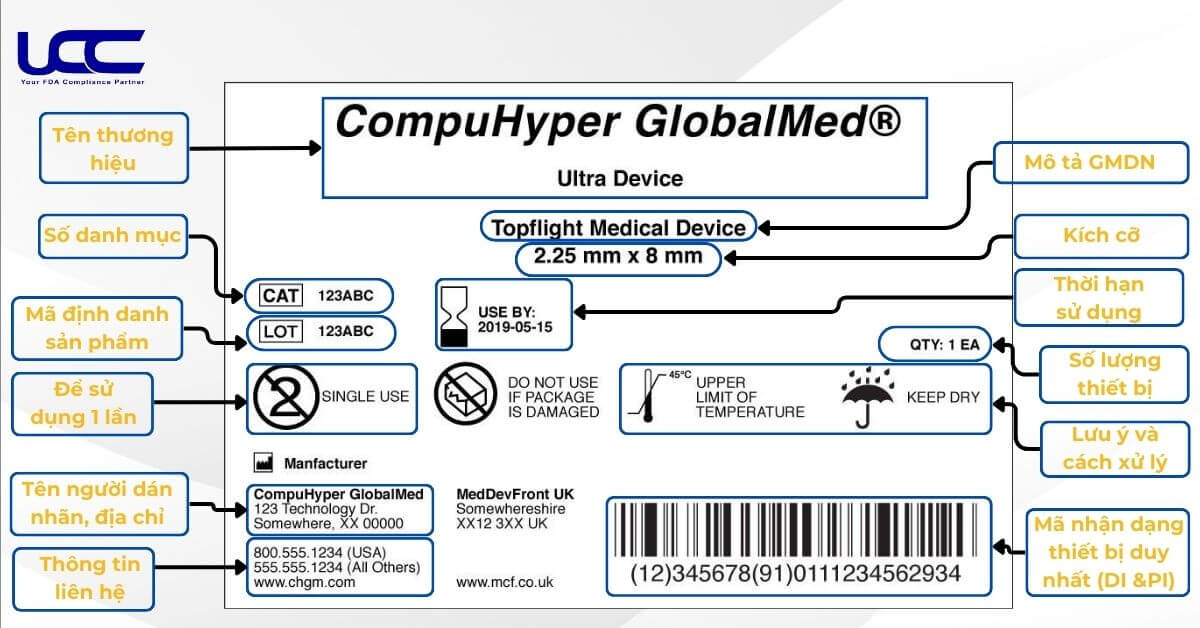
3. Một số lợi ích mà UDI mang lại
Bằng cách thiết lập hệ thống UDI để nhận dạng các thiết bị y tế thông qua phân phối. Và sử dụng cũng đã mang lại nhiều lợi ích quan trọng như:
- Giảm sai sót y tế. Sử dụng UDI để nhận dạng thiết bị một cách chính xác nhằm ngăn ngừa nhầm lẫn. Với bất kì thiết bị tương tự nào có thể dẫn đến việc sử dụng thiết bị sai mục đích.
- Đơn giản hoá việc tích hợp các thông tin sử dụng thiết bị vào hệ thống dữ liệu. UDI khi được cung cấp thông qua công nghệ AIDC. Sẽ cho phép thu thập, ghi và truy xuất dữ liệu nhanh chóng và chính xác.
- Cung cấp khả năng nhận dạng nhanh hơn các thiết bị y tế có tác dụng phụ. Việc áp dụng UDI sẽ mang lại độ chính xác cao hơn trong việc xác định các thiết bị y tế.
- Đưa ra giải pháp nhanh chóng cho các vấn đề được báo cáo. Cho phép nhà sản xuất và FDA xem xét, tổng hợp, phân tích các vấn đề tiềm ẩn. Trong các báo cáo liên quan đến thiết bị một cách nhanh chóng và đưa ra các giải pháp cho từng vấn đề.
- Thu hồi thiết bị nhanh hơn, hiệu quả hơn. Việc thu hồi thiết bị được dán nhãn UDI có thể thực hiện. Và hoàn thành càng nhanh thì sẽ giảm thiểu được những rủi ro.
4. Các quy định về UDI được đề cập trên thế giới

4.1 Hoa Kỳ
Tháng 9/2013, Cơ quan Thực phầm và Dược phẩm Hoa Kỳ (FDA) đã thiết lập hệ thống UDI. Để áp dụng cho tất cả các thiết bị y tế được bán và sử dụng tại Hoa Kỳ. Ngày 17/12/2013, GS1 đã được FDA công nhận là một trong những tổ chức cấp mã định danh thiết bị duy nhất (UDI). Tổ chức thành viên của GS1 trên toàn thế giới có nhiệm vụ. Giúp các nhà sản xuất giải quyết các yêu cầu về quy định UDI tại FDA Hoa Kỳ. Nhằm mục đích hỗ trợ an toàn cho bệnh nhân và đảm bảo an ninh chuỗi cung ứng.
Sau khi được cấp mã định danh thiết bị duy nhất phải gửi thông tin thiết bị đến Cơ sở dữ liệu nhận dạng thiết bị duy nhất toàn cầu (GUDID).
✍ Xem thêm: Tìm hiểu chi tiết về Đăng ký FDA cho cơ sở trang thiết bị y tế tại UCC Việt Nam
4.2 Châu Âu
Quy định về chuẩn đoán trong ống nghiệm (IVDR). Và Quy định về thiết bị y tế (MRD) của Châu Âu cũng đã được thông qua vào ngày 5/4/2017. Bên cạnh đó, cũng đã xác định các yêu cầu đối với hệ thống UDI của EU.
Ngày 7/6/2019, GS1 đã được Uỷ ban Châu Âu uỷ quyền là cơ quan cấp UDI. Tiêu chuẩn GS1 cho phép các nhà sản xuất trên thế giới tạo và duy trì. số UDI bằng cách tuân thủ các quy định chung của EU và GS1.
✍ Xem thêm: Tìm hiểu chi tiết về Thử nghiệm trang thiết bị y tế - Dịch vụ thử nghiệm toàn diện
5. Các câu hỏi thường gặp
Câu hỏi 1: Cơ sở dữ liệu nhận dạng thiết bị duy nhất toàn cầu (GUDID) là gì?
Cơ sở dữ liệu nhận dạng thiết bị duy nhất toàn cầu (GUDID) là cơ sở dữ liệu do FDA quản lý. Đóng vai trò là danh mục tham chiếu cho mọi thiết bị có mã nhận dạng thiết bị duy nhất (UDI). GUDID chỉ chứa phần nhận dạng thiết bị (DI) của UDI, đóng vai trò là chìa khóa để lấy thông tin thiết bị trong cơ sở dữ liệu.
Câu hỏi 2: Những sản phẩm nào phải tuân theo hệ thống UDI?
Hệ thống UDI được áp dụng cho tất cả các thiết bị. Ngoại trừ thiết bị được tùy chỉnh và các thiết bị nghiên cứu/nghiên cứu hiệu suất.
Câu hỏi 3: Có những cơ quan, tổ chức nào được FDA công nhận cấp mã UDI?
FDA đã công nhận các cơ quan phát hành sau đây:
– GS1 AISBL
– Hội đồng Truyền thông Kinh doanh Ngành Y tế (HIBCC)
– Hội đồng quốc tế về tính phổ biến trong tự động hóa ngân hàng máu (ICCBBA)
Liên hệ ngay với UCC Việt Nam để được tư vấn và hỗ trợ!





