Chứng nhận CE áo choàng phẫu thuật gói gọn trong 5 bước
Chứng nhận CE áo choàng phẫu thuật là yêu cầu bắt buộc để áo choàng phẫu thuật được bán trong thị trường Châu Âu. Chứng nhận này đảm bảo rằng áo choàng phẫu thuật đáp ứng các tiêu chuẩn an toàn, sức khỏe và hiệu quả nghiêm ngặt.
Vậy làm thế nào để áo choàng phẫu thuật được chứng nhận? Tiêu chuẩn nghiêm ngặt ra sao? Đừng bỏ lỡ, tất cả sẽ được hé lộ tất tần tật ngay tại bài viết này.
1. Quy định chung về chứng nhận CE áo choàng phẫu thuật
Sản phẩm là một thiết bị y tế để tạo rào cản giữa khu vực phẫu thuật và xung quanh. Chúng được làm từ vải không dệt polypropylene. Một loại vật liệu tổng hợp được biết với độ bền, khả năng chống rách, chống thấm.
Sản phẩm muốn lưu thông trên thị trường EU, điều kiện tiên quyết rằng phải đăng ký chứng nhận CE.
2. Quy trình xin cấp chứng nhận CE áo choàng phẫu thuật
2.1 Phân loại áo choàng phẫu thuật theo chỉ thị MDR
Áo choàng phẫu thuật thuộc loại Is tuân theo quy tắc 1 tại phụ lục VIII của quy định (EU) 2017/745.
2.2. Chuẩn bị hồ sơ xin cấp chứng nhận CE áo choàng phẫu thuật
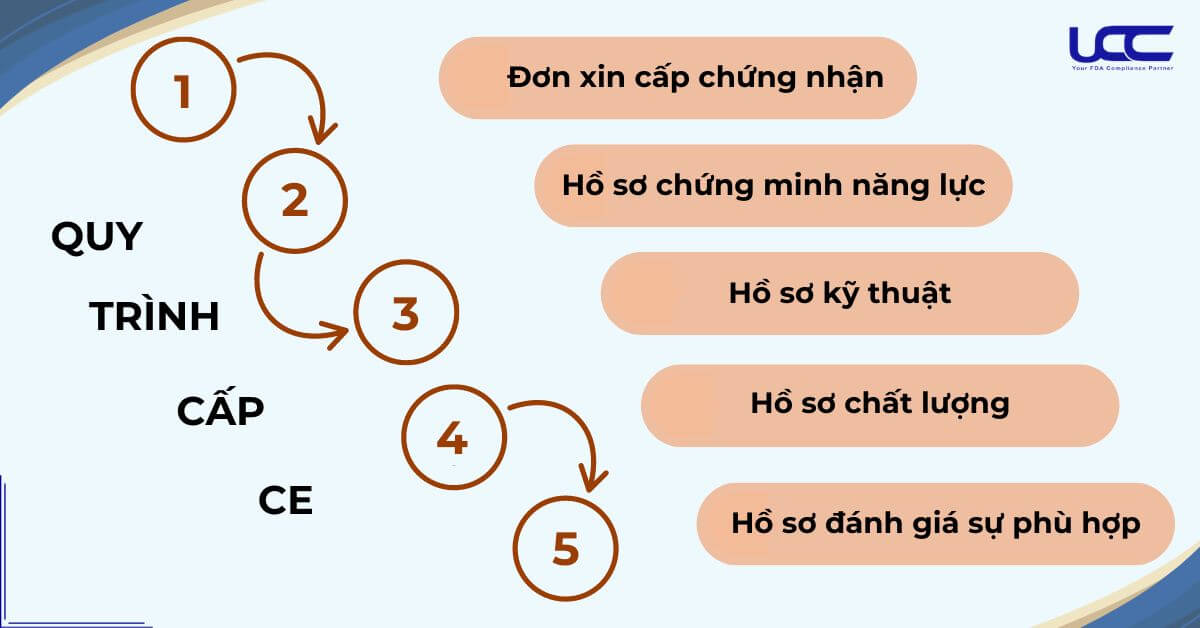
Để đáp ứng yêu cầu cấp chứng nhận CE, bao gồm các bước sau:
2.2.1. Đơn xin cấp chứng nhận
- Đơn xin cấp chứng nhận được lập theo mẫu do cơ quan quản lý có thẩm quyền quy định.
- Đơn phải được ký tên, đóng dấu đầy đủ và ghi rõ thông tin về doanh nghiệp, sản phẩm.
2.2.2. Hồ sơ chứng minh năng lực khi đăng ký chứng nhận CE áo choàng phẫu thuật
2.2.3. Hồ sơ kỹ thuật
- Mô tả chi tiết về trang thiết bị y tế: Bao gồm cấu tạo, chức năng, nguyên lý hoạt động, vật liệu sử dụng, bản vẽ kỹ thuật,…
- Hướng dẫn sử dụng và bảo quản sản phẩm: Cung cấp hướng dẫn đầy đủ và chi tiết về cách sử dụng. Bảo quản, bảo trì và vệ sinh sản phẩm.
- Kết quả thử nghiệm và đánh giá sự phù hợp: Thực hiện bởi các phòng thí nghiệm được công nhận, kết quả đánh giá rủi ro, đánh giá lâm sàng.
- Tài liệu chứng minh tuân thủ các yêu cầu an toàn, sức khỏe và bảo vệ môi trường: Cung cấp tài liệu chứng minh sản phẩm đáp ứng yêu cầu an toàn, sức khỏe.
2.2.4. Hồ sơ chất lượng
- Sổ tay chất lượng (Quality Manual): Mô tả hệ thống quản lý chất lượng của doanh nghiệp. Bao gồm quy trình, thủ tục, trách nhiệm, nguồn lực liên quan đến việc thiết kế, sản xuất, kiểm tra.
- Các thủ tục liên quan đến thiết kế, sản xuất, kiểm tra và thử nghiệm: Cung cấp đầy đủ các thủ tục, quy trình chi tiết liên quan đến từng giai đoạn.
- Hồ sơ ghi chép về hoạt động sản xuất, kiểm tra và thử nghiệm: Bao gồm các bản ghi chép về hoạt động sản xuất, kiểm tra và thử nghiệm sản phẩm. Cho phép truy xuất nguồn gốc và đảm bảo tính minh bạch của quá trình sản xuất.
2.2.5. Hồ sơ đánh giá mức độ phù hợp
- Báo cáo thử nghiệm: Cung cấp báo cáo thử nghiệm chi tiết được thực hiện bởi các phòng thí nghiệm được công nhận theo quy định.
- Báo cáo đánh giá rủi ro: Mô tả chi tiết quá trình đánh giá rủi ro cho sản phẩm, xác định các nguy cơ tiềm ẩn. Và biện pháp kiểm soát rủi ro.
- Báo cáo đánh giá lâm sàng (nếu có): Đánh giá lâm sàng chi tiết về hiệu quả và độ an toàn của sản phẩm.
- Tài liệu đáp ứng các yêu cầu thiết yếu: Chứng minh rằng sản phẩm đáp ứng các yêu cầu thiết yếu.
✍ Xem thêm: Tìm hiểu chi tiết về Chứng Nhận CE Trang Thiết Bị Y Tế Mới Nhất năm 2024
3. Các tiêu chuẩn công bố sự phù hợp chứng nhận CE áo choàng phẫu thuật
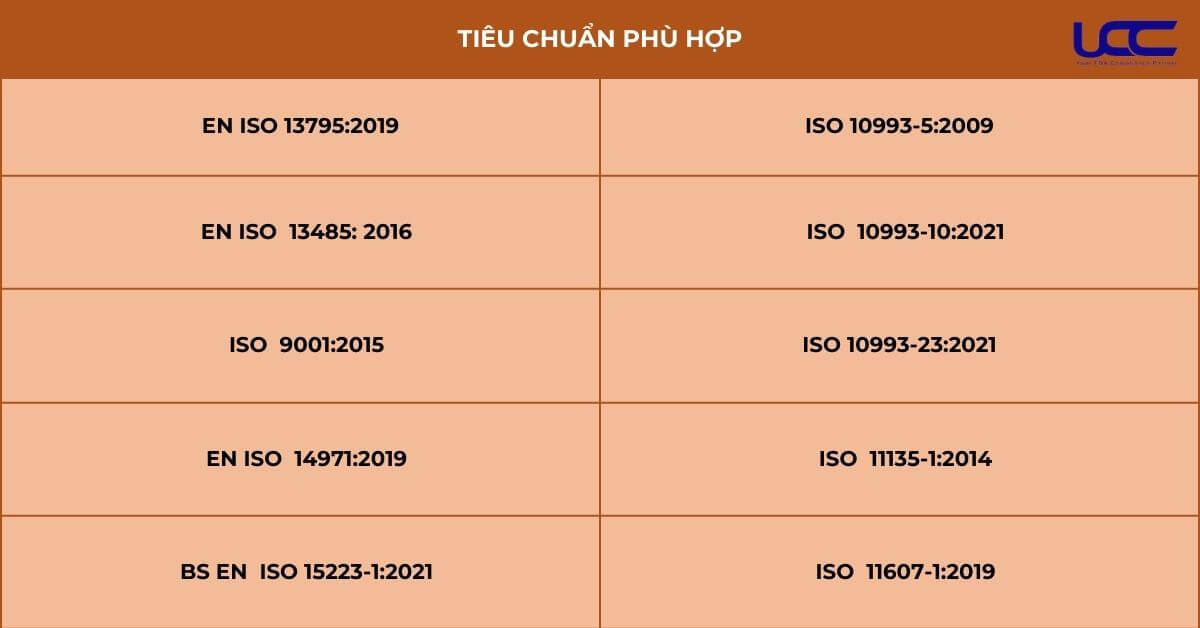
Đây là quy trình quan trọng đảm bảo sản phẩm hoặc hệ thống đăng ký chứng nhận CE áo choàng phẫu. Đáp ứng quy định về chất lượng, an toàn. Quá trình này sử dụng nhiều tiêu chuẩn khác nhau. Cụ thể đối với chứng nhận CE áo choàng phẫu thuật bao gồm một số tiêu chuẩn như sau:
4.1. EN ISO 13795:2019
Tiêu chuẩn EN ISO 13795:2019 – Quần áo và khăn trải phẫu thuật – Yêu cầu và phương pháp thử.
Quy định các yêu cầu và phương pháp thử nghiệm chứng nhận áo choàng phẫu thuật. Được sử dụng như thiết bị y tế cho bệnh nhân, nhân viên y tế và thiết bị. Nhằm ngăn ngừa lây truyền tác nhân truyền nhiễm giữa nhân viên y tế và bệnh nhân.
4.2. EN ISO 14971:2019
Tiêu chuẩn EN ISO 14971:2019 quy định các yêu cầu cho việc quản lý rủi ro trong suốt vòng đời của thiết bị y tế. Từ giai đoạn thiết kế và sản xuất đến giai đoạn sau thị trường. Mục tiêu của tiêu chuẩn này là đảm bảo rằng sản phẩm được thiết kế, sản xuất. Và sử dụng một cách an toàn cho bệnh nhân, người sử dụng và bên thứ ba.
4.3. ISO 10993-5:2009
ISO 10993-5:2009 – Đánh giá sinh học về thiết bị y tế – Phần 5: Xét nghiệm độc tính tế bào in vitro.
Tiêu chuẩn ISO 10993-5:2009 quy định các phương pháp thử nghiệm để đánh giá độc tính tế bào in vitro của thiết bị y tế. Mục đích để xác định khả năng gây hại tiềm ẩn đối với tế bào và mô của cơ thể.
4.4. ISO 10993-23:2021
ISO 10993-23:2021 – Đánh giá sinh học về thiết bị y tế – Phần 23: Thử nghiệm kích ứng
Tiêu chuẩn ISO 10993-23:2021 để đánh giá khả năng gây kích ứng da của thiết bị y tế và vật liệu khi tiếp xúc với da. Mục đích của tiêu chuẩn này là đảm bảo rằng thiết bị y tế không gây ra phản ứng da bất lợi cho người sử dụng.
4.5. ISO 11135-1:2014
ISO 11135-1:2014 – Tiệt khuẩn sản phẩm chăm sóc sức khỏe – Etylen oxit – Phần 1: Yêu cầu cho việc phát triển, xác nhận và kiểm soát thường xuyên quy trình tiệt khuẩn đối với thiết bị y tế.
Tiêu chuẩn ISO 11135-1:2014 quy định các yêu cầu cho việc phát triển, xác nhận và kiểm soát. Mục đích đảm bảo rằng thiết bị y tế được tiệt khuẩn một cách hiệu quả và an toàn bằng EtO.
4.6. ISO 11607-1:2019
ISO 11607-1:2019 – Bao bì cho thiết bị y tế đã được tiệt khuẩn bằng phương pháp cuối cùng – Phần 1: Yêu cầu đối với vật liệu, hệ thống rào cản và hệ thống bao bì.
Quy định đối với vật liệu, hệ thống rào cản và hệ thống bao bì cho thiết bị y tế. Chúng đã được tiệt khuẩn bằng phương pháp cuối cùng. Mục đích đảm bảo rằng thiết bị y tế được bảo vệ khỏi sự nhiễm bẩn và hư hỏng khi chứng nhận CE áo choàng phẫu thuật.
4.7. ISO 11607-2:2019
ISO 11607-2:2019 – Bao bì cho thiết bị y tế đã được tiệt khuẩn bằng phương pháp cuối cùng – Phần 2: Yêu cầu xác nhận quy trình đóng gói
Quy định yêu cầu xác nhận quy trình đóng gói cho thiết bị y tế đã được tiệt khuẩn bằng phương pháp cuối cùng. Đảm bảo khỏi sự nhiễm bẩn và hư hỏng trong suốt quá trình vận chuyển, lưu trữ và sử dụng.
4.8. EN 556-1:2001
EN 556-1:2001 – Tiệt khuẩn thiết bị y tế.
Quy định đối với thiết bị y tế được tiệt khuẩn cuối cùng để được đánh dấu “vô trùng”. Mục đích rằng thiết bị y tế được tiệt khuẩn một cách hiệu quả và an toàn. Đáp ứng các yêu cầu về tính toàn vẹn và hiệu quả chứng nhận CE áo choàng phẫu thuật.
4.9. MDR EU 2017/745
Quy định về thiết bị y tế (MDR) EU 2017/745, có hiệu lực từ ngày 26 tháng 5 năm 2021. Thay thế Chỉ thị về thiết bị y tế (MDD) 93/42/EEC cũ. MDR nhằm nâng cao chất lượng, độ an toàn khi đăng ký chứng nhận CE áo choàng phẫu thuật.

5. Chứng nhận CE áo choàng phẫu thuật giúp gia nhập thị trường EU
Chứng nhận CE áo choàng phẫu thuật là một yếu tố quan trọng khi gia nhập vào thị trường EU. Việc có được nhãn CE cho thấy rằng sản phẩm đã đáp ứng các yêu cầu nghiêm ngặt. Doanh nghiệp nên đầu tư kiểm định CE để nâng cao hiệu quả kinh doanh trên thị trường.
UCC Việt Nam với đội ngũ nhân viên có kinh nghiệm về lĩnh vực chứng nhận chất lượng cho trang thiết bị y tế. Chúng tôi cam kết mang đến dịch vụ uy tín và tốt nhất cho doanh nghiệp.
Trên đây là những thông tin cần biết về hoạt động chứng nhận CE áo choàng phẫu thuật. Mọi thông tin cần hỗ trợ, quý khách hàng vui lòng liên hệ UCC VIỆT NAM qua Hotline 036 790 8639 email admin@ucc.com.vn để được UCC Việt Nam hỗ trợ!
Xem thêm: Chứng nhận FDA áo choàng phẫu thuật – Uy tín nhanh chóng
Tin tức liên quan










